【GCP快讯】凝聚共识促发展,优化流程启新篇 ——中山一院药物临床试验机构召开临床试验企业座谈交流会
领航聚力,共谋发展
为进一步优化我院临床试验全流程管理,提升多方协作效率,在中山大学附属第一医院精准研究院常务副院长、药物临床试验机构主任彭穗教授的指导下,我院药物临床试验机构于2025年5月16日成功举办"企业座谈交流会",来自19家国内外知名申办方、CRO及SMO公司的30余名代表,与药物临床试验机构副主任唐蕾教授及机构办工作人员展开深度对话,共绘临床试验高质量发展蓝图。


流程革新:从"串联"到"并联"的智慧跃迁
自2023年下半年起,在机构领导班子的前瞻部署下,我院突破传统"串联式"流程的桎梏,创新构建"伦理-合同-遗传办"三项并行的管理新模式,在立项后即可同步启动多环节筹备,加速项目启动速度。药物临床试验机构立项专员/HGR专员蔡承晖详细介绍了中山一院药物临床试验机构高效的启动前流程:机构1天内回复立项前调研邮件;1-2天完成立项受理;立项完成后,同步开放合同审核、伦理审查及遗传办审批通道,在合同洽谈过程中还可同步进行启动前质控预约和CTMS系统方案配置,项目平均启动周期大幅缩短。
在深化流程改革的过程中,我院以申办方需求为导向,实现关键环节的精细化升级。针对立项与遗传办环节中需要PI签字、申办方盖章的材料,允许企业在确保文件合规的前提下,将补充材料时间延至启动前。
同时,依托数字化工具实现机构和申办方之间更加高效的沟通。遗传办材料可以通过邮件进行线上形审及问题反馈,避免重复签字或盖章递交。
本月中旬即将上线的智能合同迭代升级系统,将集成“模板一键调取、合同线上审核、检查检验费随时查询、费用自动计算”四大功能,实现"数据多跑腿、企业零等待"。特别是“检查检验费随时查询”功能:申办方可直接在外网环境下通过CTMS系统随时随地、一目了然地查阅我院所有检查检验组套及其对应费用明细。这一高效便捷的自助查询方式赢得了申办方的高度赞扬。

质控升级:全周期闭环管理护航数据质量
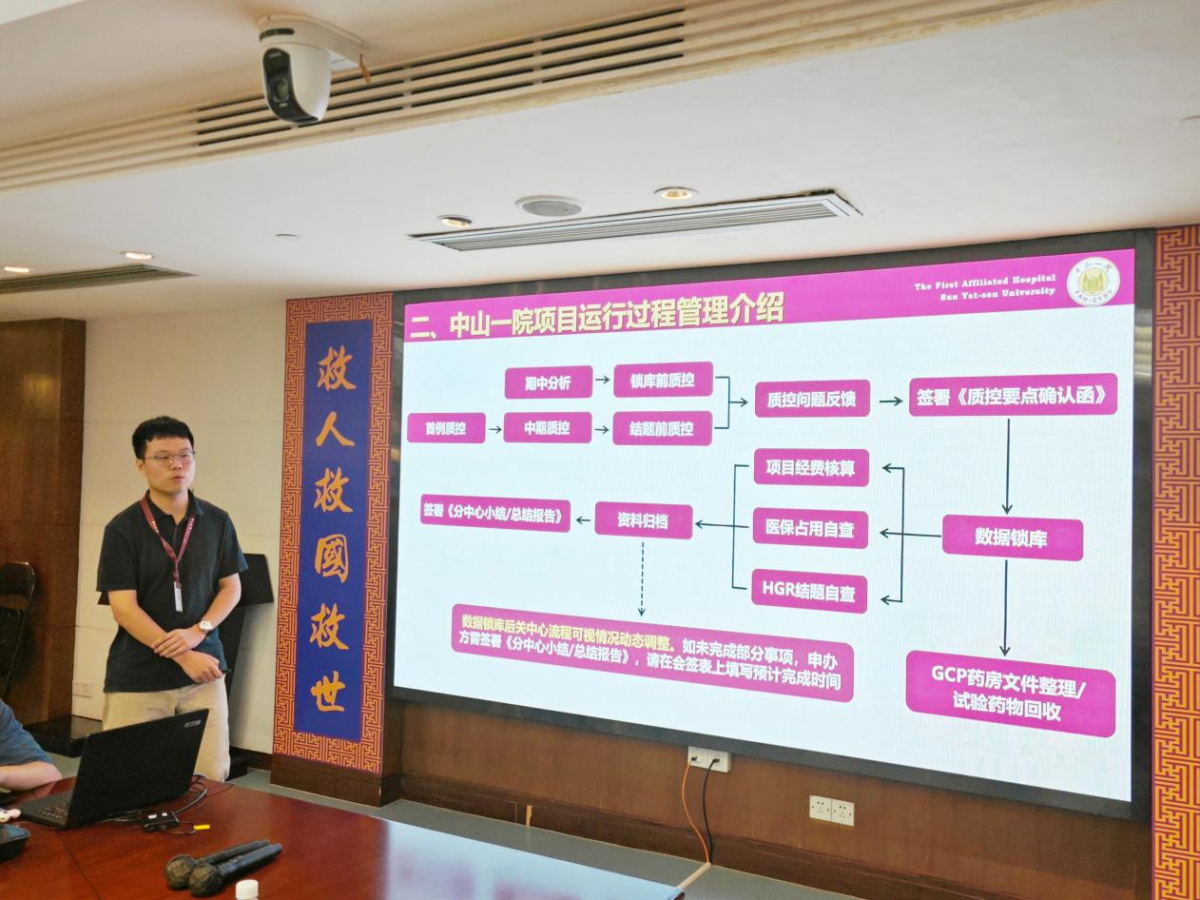
质控员彭健系统阐述我院临床试验项目运行过程的管理实践,,重点介绍了中山一院在首例入组、中期及结题前等关键环节的基于风险的质控与优化措施,保障项目高效规范推进。唐蕾主任高度关注项目锁库速度,通过早会不断提醒质控员密切关注项目进展。机构办质控员在获悉锁库计划或末例患者完成主要疗效指标评估后即刻启动锁库前质控流程,将发现和解决问题的时间点大幅提前,实现“质控前置、风险早排”新范式,确保锁库前质控流程不会延误锁库时间,甚至可以在预期时间前完成,成功平衡申办方效率需求与机构质量要求,保证递交国家药监局的数据真实、可靠、可溯源。此外,关中心流程可根据实际情况进行动态调整。
经验共享:企业代表分享伦理材料‘一次做对’黄金法则
阿斯利康公司资深临床研究监查员王红在分享环节中,以多年实战经验梳理了伦理审查资料准备的优化路径。她指出,文件规范性是伦理审查的“第一道门槛”,针对递交信、自查表及知情同意书中常见的格式错误和内容不规范等问题,强调需精读伦理委员会递交指引,逐项核验文件内容的完整性与表述严谨性,尤其需从伦理审查视角对文件进行自查。针对CTMS系统操作痛点,王红讲解了文件上传和填写的要点。此外,她还强调了主动沟通的重要性,将被动修改化为主动沟通,有助于提高伦理初审的通过效率。"最高效的秘诀不是快速修改,而是一次做对。"阿斯利康的经验总结引发与会企业强烈共鸣。下期推文我们将详细介绍“一次做对”黄金法则的实践路径。

共话未来:开放问答书写临床试验新篇章
在座谈交流环节,申办方代表就伦理审查与机构启动流程展开了深度探讨。唐蕾主任携团队即时回应关切问题,并将合理化建议纳入改进清单。面向行业高质量发展新阶段,我们诚邀业界伙伴:共建标准化流程体系,打造无界化沟通机制,探索智能化质控模式。以创新协作模式加速研发进程,让更多突破性疗法早日守护生命健康。勠力同心,共赴医疗创新的星辰大海!





